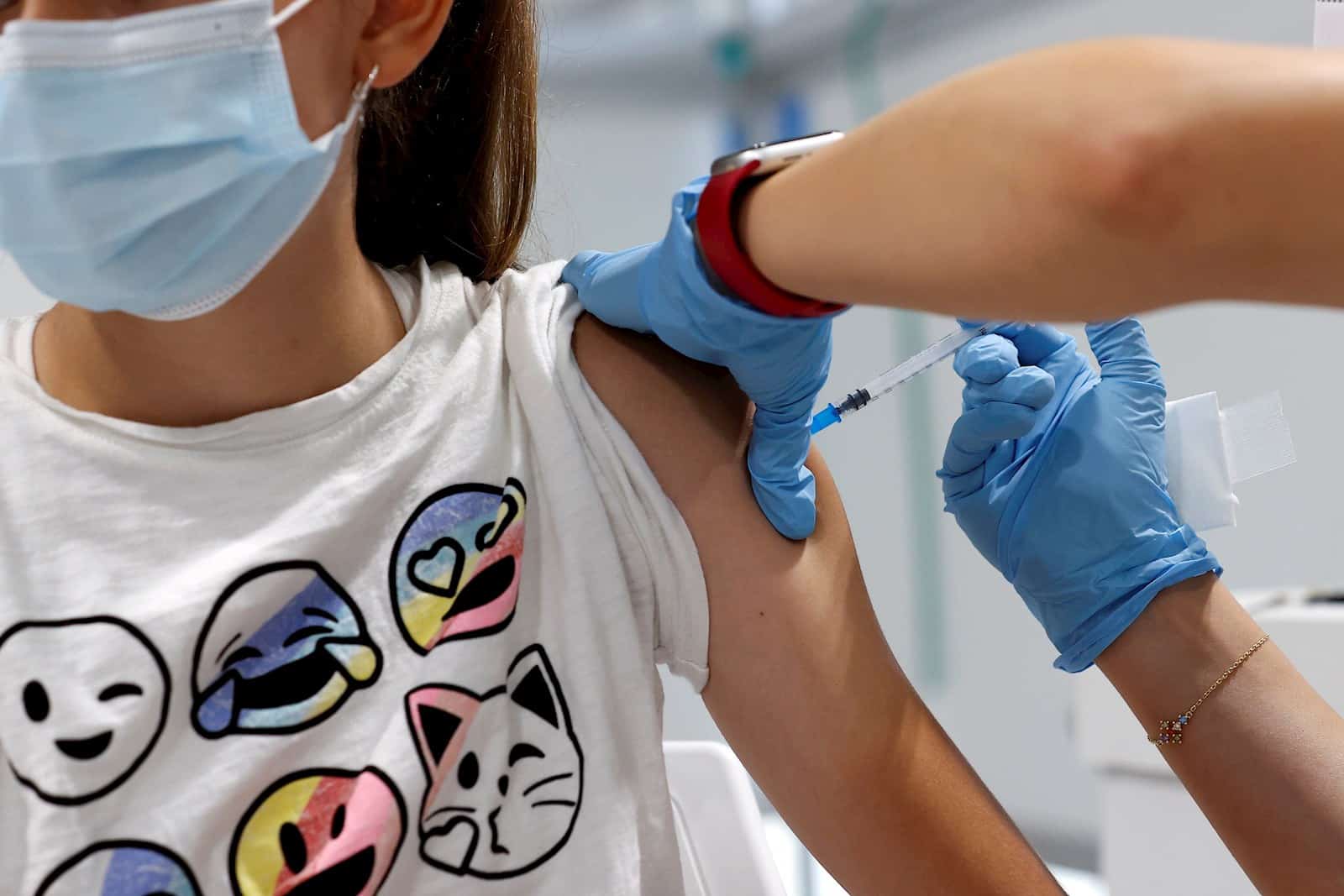
- Las empresas Moderna y Pfizer/BioNTech se encuentran en ensayo de las vacunas para niños entre 5 y 11 años de edad
La propagación de los contagios por la variante delta del covid-19 y el posible regreso a clases presenciales mantienen a algunos padres y representantes preocupados, puesto que los más pequeños aún no son elegibles para ser inmunizados.
Las vacunas contra el covid-19 para niños menores de 12 años de edad aún no han sido aprobadas por la Organización Mundial de la Salud (OMS), debido a que no han concluido los ensayos para conocer la seguridad de la inmunización en ese rango de edad.
“No se dispone de datos sobre la eficacia o la seguridad de la vacuna en los niños menores de 12 años. Hasta que se disponga de esos datos, no se recomienda vacunar sistemáticamente a este grupo de edad”, indica la OMS.
No obstante, algunos laboratorios se encuentran en la fase de ensayo. Cuando las compañías tengan los resultados del estudio deberán enviarlo a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) para su evaluación y autorización.
También te recomendamos
Pfizer/BioNTech y Moderna en ensayos
Las empresas Moderna y Pfizer/BioNTech iniciaron a principios del año 2021 los ensayos clínicos de las vacunas para niños menores de 12 años.
Se estima que la dosis del laboratorio Pfizer, la cual se encuentra en fase III, sea la primera en obtener los resultados y próximamente solicite su autorización a la FDA.
El doctor Scott Gottlieb, excomisionado de la FDA y miembro de la junta de Pfizer, indicó que la compañía probablemente podrá presentar los datos de los resultados en niños de 5 a 11 años, solicitar la autorización a mediados de septiembre y luego emitir la solicitud en octubre para su uso de emergencia.
“Eso nos pondrá en un marco de tiempo en el que las vacunas podrían estar disponibles en algún momento a fines del otoño, más probablemente a principios del invierno, dependiendo de cuánto tiempo demore la FDA en revisar la solicitud”, dijo en entrevista para el programa estadounidense Face the Nation de CBS el 29 de agosto.
El exjefe de la FDA precisó que existe la posibilidad de que el cronograma cambie en caso de que el ente regulador de medicamentos decida que quiere un seguimiento de tres a seis meses de los niños en los ensayos clínicos.
Sin embargo, indicó que la variante delta ha provocado un resurgimiento de casos de coronavirus, hospitalizaciones y muertes, lo que podría acelerar el proceso de revisión de la vacuna en los niños más pequeños.
“Si continuamos viendo estas tasas cada vez mayores de infecciones en los niños, particularmente a medida que la variante delta se traslada al noreste, creo que podría haber más presión para intentar hacer una autorización más temprana para una vacuna”, dijo Gottlieb.
Por otra parte, reveló que los datos del ensayo de Pfizer en niños menores de 5 años no se enviarán hasta probablemente noviembre. Detalló que la dosis para ese rango de edad es más baja.
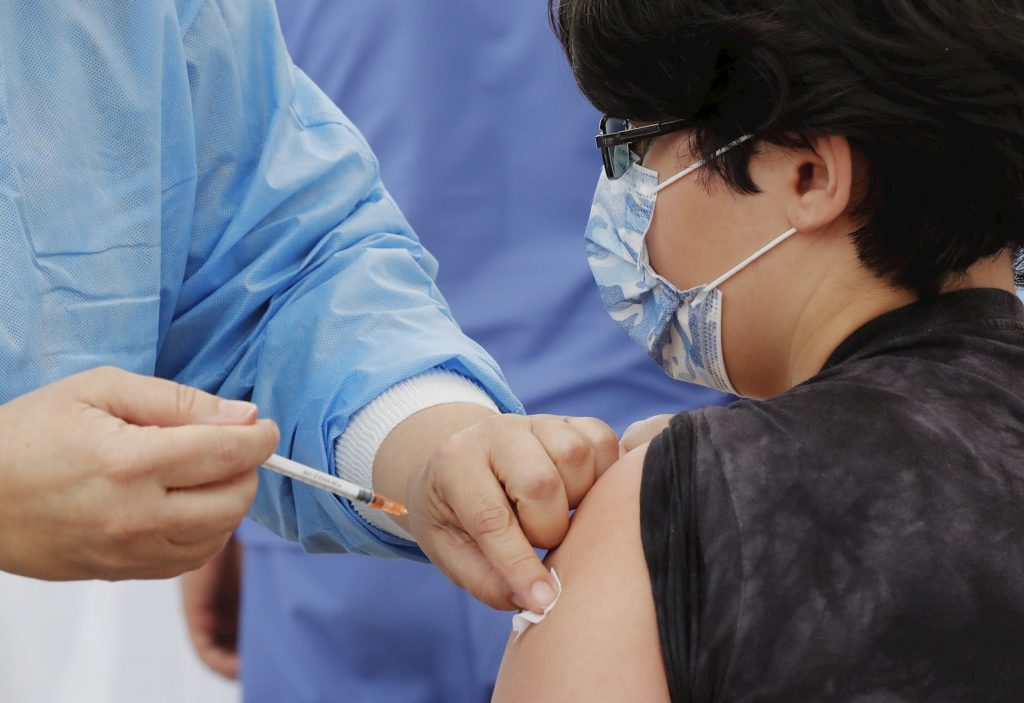
Moderna amplía número de participantes
El diario estadounidense The New York Times reseñó que la FDA pidió a las empresas que incluyan a 3.000 niños en el grupo de 5 a 11 años. No obstante, un portavoz de Moderna, Ray Jordan, confirmó que la compañía tiene la intención de expandir su prueba para inscribir una base de datos de seguridad más grande que aumenta la probabilidad de detectar eventos fuera de lo normal.
Moderna comenzó a reclutar pacientes para su ensayo en marzo de 2021 con el objetivo de inscribir a 6.795 participantes menores de 12 años. Los voluntarios debían dividirse en partes iguales en tres grupos de edad.
El laboratorio espera buscar autorización de emergencia a fines de este año o principios del próximo.
Covid-19: vacunas para mayores de 12 años de edad
La OMS detalló que en un ensayo de fase III en el que se incluyó a niños de 12 a 15 años de edad, se observó que la vacuna era muy eficaz y bastante segura, por lo que decidió aprobar la inmunización en este grupo.
“Se recomienda que los países administren la vacuna a los niños de 12 a 15 años solo cuando se haya alcanzado una alta cobertura vacunal con las dos dosis en los grupos de máxima prioridad”, precisó.
Además indicó que se debe ofrecer la vacunación a los niños de 12 a 15 años que presenten enfermedades concurrentes que aumenten significativamente el riesgo de sufrir síntomas graves del virus.
La Agencia Europea de Medicamentos (EMA) aprobó el 28 de mayo el uso de la vacuna de Pfizer a partir de los 12 años de edad y el 23 de julio autorizó el empleo del fármaco de Moderna para el grupo de 12 a 17 años.
El organismo concluyó que los beneficios de la vacunación superaban los riesgos. Entre los efectos secundarios más comunes están: dolor de cabeza o en el lugar de la inyección, cansancio, dolor muscular y articular, escalofríos y fiebre, los cuales mejoran a los pocos días.
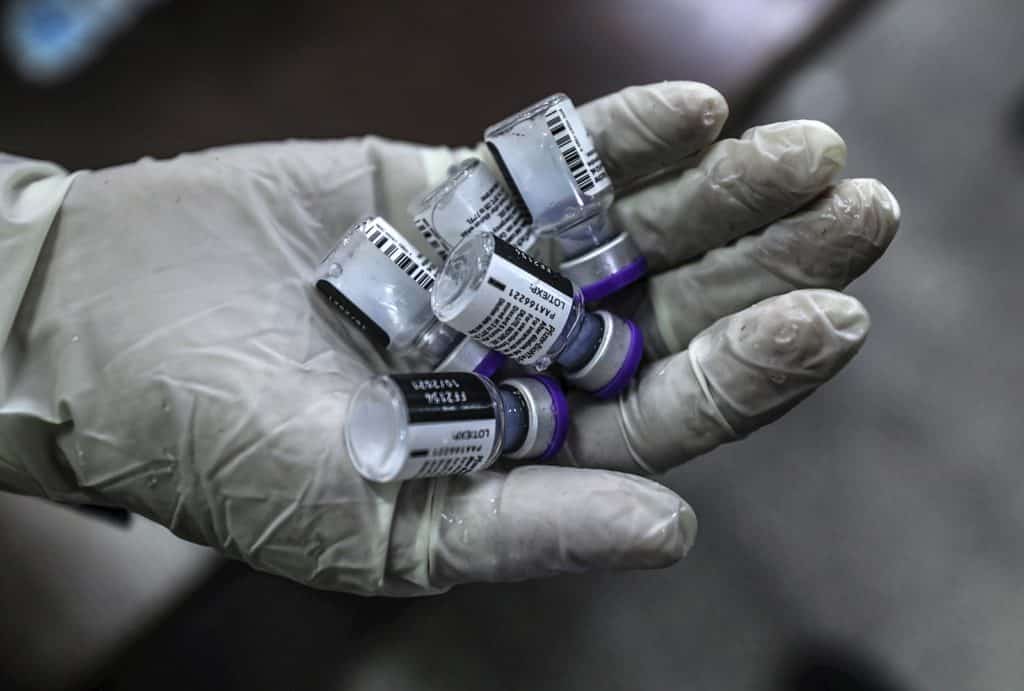
Países que autorizaron vacunar contra el covid-19 a menores de 12 años
En junio de 2021, China autorizó el uso de la vacuna de Sinopharm y Sinovac en niños de 3 a 12 años, luego de completar las fases 1 y 2 de ensayos en ese grupo de la población.
De acuerdo con la agencia de noticias oficial Xinhua, los antígenos desarrollados por las farmacéuticas Sinopharm y Sinovac demostraron ser seguros en niños, niñas y adolescentes.
El presidente de la farmacéutica Sinovac, Yin Weidong, detalló la fase I y II de los ensayos involucró cientos de voluntarios en este grupo de edad y los resultados revelaron que la vacuna es tan segura y eficiente como lo es para los adultos,
En agosto, el Ministerio de Salud de Emiratos Árabes Unidos también aprobó la vacunación contra covid-19 en niños de entre 3 y 17 años con la vacuna china de Sinopharm después de haber comprobado su efectividad.
El Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos (Cecmed) de Cuba anunció el 3 de septiembre que autorizó el uso de emergencia para inocular a la población pediátrica con la vacuna Soberana 02.
La agencia de noticias EFE reseño que el Instituto Finlay de Vacunas realizó el ensayo clínico u0022Soberana Pediatríau0022 con 350 niños de La Habana de entre 3 y 18 años de edad.
El estudio demostró un 91,2 % de eficacia contra la enfermedad sintomática en su análisis de la fase III, según la institución científica.
Este 6 de septiembre, el Instituto de Salud Pública de Chile indicó que la vacuna de la farmacéutica china Sinovac se aprobó para su uso de emergencia en niños mayores de 6 años.
Chile no permite la salida de país de niños sin vacuna
Desde el 26 de julio comenzó a funcionar en Chile el Plan de Fronteras Protegidas, en el que se estableció que las personas solo pueden salir del país si tienen el Pase de Movilidad habilitado, el cual se obtiene si cuentan con las dos dosis de la vacuna.nnPor ende, los niños, niñas y adolescentes no vacunados no podrán salir del país. Sin embargo, se puede brindar un permiso especial en casos humanitarios o de salud, de acuerdo con las subsecretarías de Salud Pública y Prevención del Delito, Paula Daza y Katherine Martorell.nn“Todas las personas pueden requerir en casos excepcionales la solicitud a Comisaría Virtual, pero deben acreditar esa situación excepcional”, expresó Martorell.n
Desde el inicio de la pandemia se han registrado más de 220.990.240 casos de covid-19 y al menos 4.573.126 muertes. Estados Unidos, India e Irán continúan siendo los países con más contagiados.
Hasta la fecha, el 40.4% de la población mundial ha recibido al menos una dosis de la vacuna contra el covid-19 y se han administrado 5.49 billones de dosis en total, de acuerdo con Our World In Data.