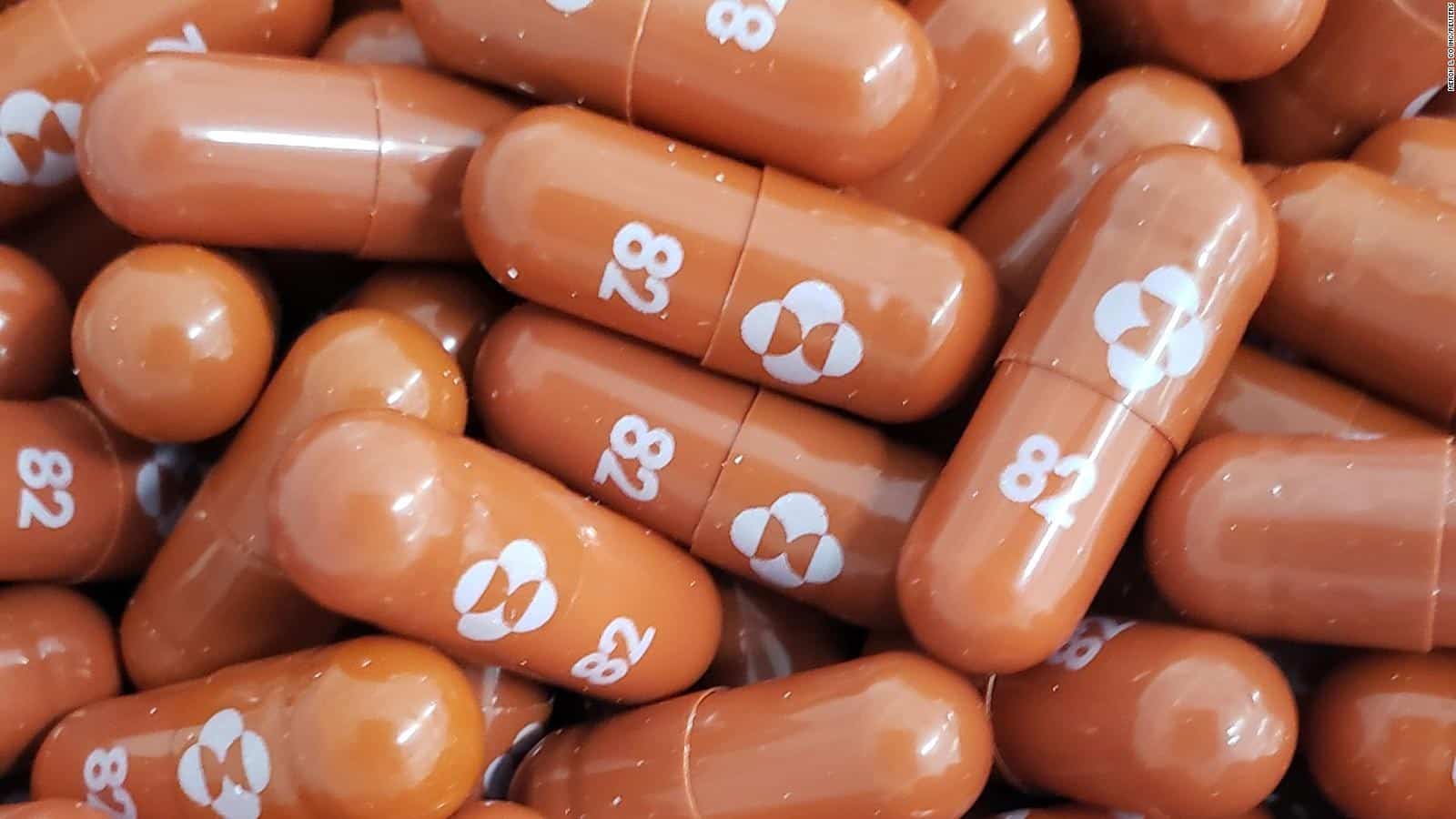
- El medicamento fabricado por la farmacéutica Merck & Co mostró una reducción de 50% en los riesgos de hospitalización de pacientes contagiados con covid-19
La farmacéutica estadounidense Merck & Co anunció que su píldora molnupiravir redujo muertes y hospitalizaciones por covid-19 en su etapa de estudio. La compañía, en asociación con Ridgeback Biotherapeutics, envió los resultados de los ensayos a la Administración de Medicamentos y Alimentos (FDA, por siglas en inglés) y a la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) para solicitar la autorización de uso de emergencia en los Estados Unidos.
Las dos empresas aseguraron el viernes 1° de octubre que el ensayo clínico provisional fue un éxito, ya que mostró una reducción de 50% en las posibilidades de internar al paciente y también en los riesgos de muerte por coronavirus. Las farmacéuticas además aclararon que los resultados son preliminares, “pero impresionantes”.
Detalles de la investigación
Merck & Co y Ridgeback Biotherapeutics revelaron que la diferencia entre las personas con síntomas de covid-19 que tomaron el fármaco y las que ingirieron el placebo fue “muy marcada”. De 775 pacientes solo 7,3% de los que recibieron molnupiravir fueron hospitalizados, una cifra más satisfactoria que el 14,1% de los que tomaron placebo.

Además, no hubo muertes en el grupo que tomó la píldora de Merck, pero sí hubo ocho personas que fallecieron con el placebo. En la investigación se incluyeron pacientes de casi todo el mundo, con cuadros de coronavirus leves y moderados que tenían síntomas que no pasaban los cinco días.
A los participantes se les suministró una píldora (de molnupiravir o placebo) cada 12 horas durante cinco días. Todos los sujetos tenían un factor de riesgo como obesidad o edad avanzada.
La farmacéutica Merck comentó que la secuenciación viral hasta el momento muestra que el nuevo medicamento es eficaz contra todas las variantes, incluyendo la Delta. No obstante, la empresa omitió detalles sobre los efectos secundarios del medicamento.
La fase 3 de los ensayos se interrumpieron mientras se espera una respuesta de la FDA. Por su parte, la EMA anunció que en los “próximos días” iniciará una revisión del fármaco para corroborar los resultados, mientras que la Organización Mundial de la Salud (OMS) no ha emitido su opinión al respecto.
Lo que se sabe de la molnupiravir
El fármaco afecta directamente el código genético del virus. Esta característica lo podría convertir en el medicamento pionero, dentro de los antivirales orales, en combatir al covid-19.
En la carrera por crear una píldora que contrarreste los síntomas del coronavirus están también las farmacéuticas Pfizer y Roche Holding AG. Sin embargo, aún no se ha avanzado en estos estudios.
Entre las ventajas de la molnupiravir está que se puede almacenar y distribuir fácilmente, además de ser sencilla y económica de fabricar. Se puede ingerir dentro de los cinco días posteriores a los primeros síntomas.
La farmacéutica Merck espera producir antes de que finalice 2021, 10 millones de tratamientos completos (lo que equivale a 40 pastillas por paciente), así como también lograr un acuerdo en abril 2022 para licenciar su fórmula a otros fabricantes de genéricos con el fin de aumentar el suministro global.
La compañía confía en poder ofrecer a las naciones de bajos recursos precios más bajos de los 700 dólares por tratamiento. Cifra que pagará Estados Unidos por las más de un 1,7 millones de dosis que ya acordó comprar.
La aprobación del medicamento se espera para finales de 2021. La empresa Merck apuesta porque los países ricos y las organizaciones mundiales de salud pública financien la fabricación de molnupiravir para así garantizar que los medicamentos se distribuyan ampliamente.

¿Qué otros ensayos se realizaron para encontrar un tratamiento?
Más de 150 fármacos diferentes fueron investigados en 2020 en distintos países del mundo. La mayoría fueron estudios sobre medicamentos existentes.
Por ejemplo, Reino Unido llevó a cabo un ensayo clínico llamado Recovery, con 12.000 pacientes. Fue uno de los pocos ensayos que dio una visión definitiva sobre qué medicamentos están funcionando y cuáles no.
La Organización Mundial de la Salud (OMS) realizó un estudio bautizado como Solidaridad, para evaluar los tratamientos que demostraron ser promisorios en distintos países del mundo.
Sin embargo, los resultados no fueron 100% eficaces y muchos de los ensayos se suspendieron. Es por ello, que actualmente la apuesta es a la píldora de la farmacéutica Merk, que de acuerdo con sus estudios, es la que podría aprobarse como medicamento oficial contra el covid-19.