- Los investigadores esperan que la Agencia Española del Medicamento autorice la aplicación del fármaco en humanos. El trámite retrasa la primera fase de ensayos clínicos, para el que ya había comenzado la preselección de voluntarios. Otros candidatos vacunales como Novavax, CanSino y Curavac siguen en la fase 3 de pruebas
El Consejo Superior de Investigaciones Científicas de España (CSIC) anunció el sábado 31 de julio de 2021 que se paralizó la fase de pruebas en humanos de su candidata a vacuna contra el covid-19. En un comunicado, informó que la Agencia Española del Medicamento (Aemps) todavía no autoriza el comienzo de los ensayos clínicos.
La vacuna MVA-COVID-19(S) fue desarrollada por el Centro Nacional de Biotecnología (CNB) de ese país, junto al laboratorio privado Biofabri. Usa como base una versión genéticamente modificada del Vaccinia virus, el cual es utilizado para las vacunas contra la viruela. La fórmula ya había demostrado tener 100% de efectividad en ratones de laboratorio, además de aprobar las pruebas en diferentes especies de monos.
Todavía se desconoce la razón por la que la Aemps aún no da luz verde a las pruebas del fármaco en humanos. El retraso obligó a los investigadores a suspender la fase 1 de ensayos clínicos que ya estaban programados para iniciar a finales de agosto en el Hospital Universitario La Paz, en Madrid. El centro estaba reclutando voluntarios entre 19 y 39 años que no hubieran recibido previamente vacunas contra el coronavirus.
Desmienten muerte de mono

Uno de los primeros medios de comunicación en informar sobre la paralización de las pruebas fue el portal El Español. Allí se aseguró que la suspensión indefinida se debía a la muerte por lesión pulmonar de 1 de los 12 macacos utilizados en los ensayos finales.
No obstante, el investigador del CNB-CSIC Mario Esteban aseguró en entrevista con el diario español ABC que ningún primate murió durante el proceso. “Es totalmente falso que la administración de la vacuna haya producido la muerte por lesiones pulmonares de uno de los macacos utilizados en los ensayos preclínicos”, declaró .
De acuerdo con lo reseñado por ABC, el propio CSIC en su comunicado desmintió la información y acotó que solo esperan la autorización de la Aemps para avanzar en los ensayos clínicos. “Si se hubiera producido la muerte de un macaco tras la administración de la vacuna, no se hubiera solicitado el ensayo clínico”, declaró.
Otros aspirantes
Actualmente el mundo atraviesa una fase de vacunación contra el covid-19, luego del desarrollo de diferentes fórmulas por parte de diferentes centros de investigación estatales y privados. Vacunas como las desarrolladas por Moderna, Pfizer-BioNTech, Sinopharm o la rusa Sputnik V ya se aplican masivamente en todos los países. Sin embargo, todavía quedan varios laboratorios experimentando para sus propias versiones.
Entre las vacunas que todavía se encuentran en la fase 3 de ensayos clínicos está la creada por la empresa alemana Curavac. Se basa en la misma tecnología que las de Moderna y Pfizer-BioNTech, aunque con la ventaja de que se puede conservar en refrigeradores normales. A finales de junio la biofarmacéutica anunció que tras los análisis en 40.000 sujetos de prueba, la vacuna mostró solo un 47% de eficacia general contra el coronavirus. “No se han cumplido los criterios estadísticos de éxito”, reconoce Curavac en su estudio.
Recientemente la OMS autorizó el uso en casos de emergencia de la vacuna de la empresa Sinovac. Se suma a Sinopharm como las opciones de China para combatir al coronavirus. Una aspirante a ser la tercera aprobada es el fármaco de la empresa CanSino, que en su fase 3 de ensayos clínicos obtuvo 68,83% de eficiencia general. Aunque no tiene un reconocimiento oficial, ya ha sido permitida por algunos gobiernos como el de México.
Candidato prometedor
La empresa de biotecnología Novavax asegura haber comenzado el desarrollo de su vacuna desde que se conocieron los primeros brotes de covid-19 en el mundo. De acuerdo con información de CNN, la fórmula de Novavax utiliza una proteína S recombinante similar a la del virus SARS-Cov-2 (causante del covid-19), para que los anticuerpos generen inmunidad, además del adyuvante Matrix-M, que estimula la respuesta inmune del organismo.
Resultados preliminares de la fase 3 realizados en Reino Unido demostraron que la vacuna cuenta con una eficacia general de 89,7% luego de ser actualizada para combatir las diferentes variantes del virus. Igualmente presenta 86,3% de efectividad frente a la variante alfa detectada a finales de 2020 en ese país.
El comité asesor de vacunas de la Asociación Española de Pediatría considera que la vacuna de Novavax es una de las más prometedoras hasta ahora entre los candidatos en fase 3. Todavía no se han publicado los resultados definitivos de sus ensayos clínicos; sin embargo, se espera que agencias como la OMS o la FDA pudieran darle el visto bueno en el tercer trimestre de 2021.
Resultados dudosos
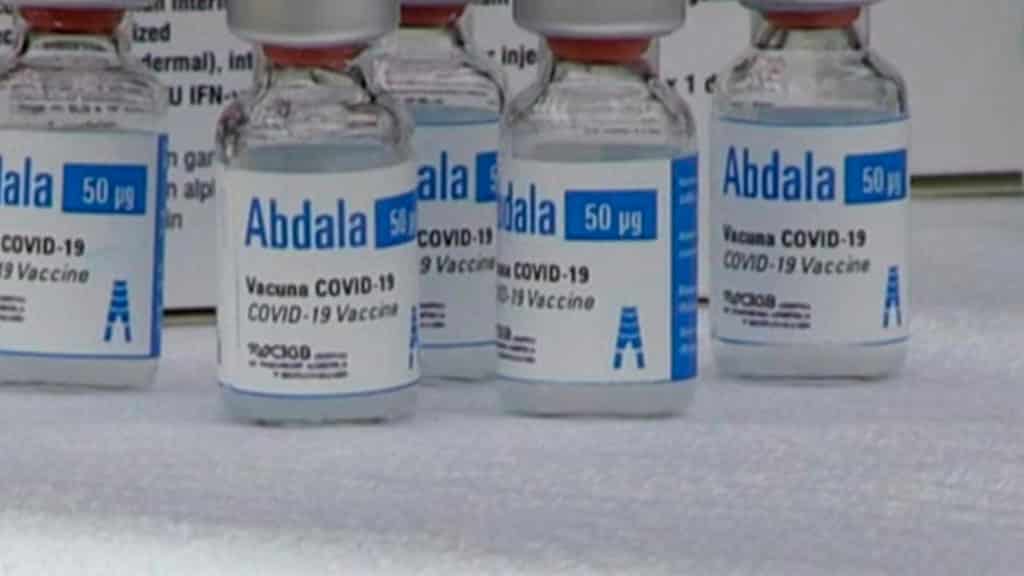
Una vacuna experimental ampliamente conocida en Venezuela es la Abdala, creada por el Centro de Ingeniería Genética y Biotecnología de Cuba (CIGB). El régimen de Nicolás Maduro anunció el 24 de junio de 2021 la adquisición de 12 millones de dosis para el Plan Nacional de Vacunación.
Diferentes instituciones rechazaron la medida, entre ellas la Academia Nacional de Medicina, la organización Médicos Unidos por Venezuela, la Asociación de Investigadores del Instituto Venezolano de Investigaciones Científicas (Asoinivic) y el Centro Nacional de Bioética (Cenabi). Todos manifestaron su preocupación por la aplicación en la población de una vacuna que no está autorizada por la OMS. Tampoco posee resultados creíbles avalados por instituciones científicas internacionales.
Hasta el momento Cuba ha presentado cinco candidatas a vacuna contra el covid-19: la Abdala, Soberana 01, Soberana 02, Soberana Plus y Mambisa. Ninguna tiene la aprobación de la OMS ni de centros de investigación científica reconocidos.