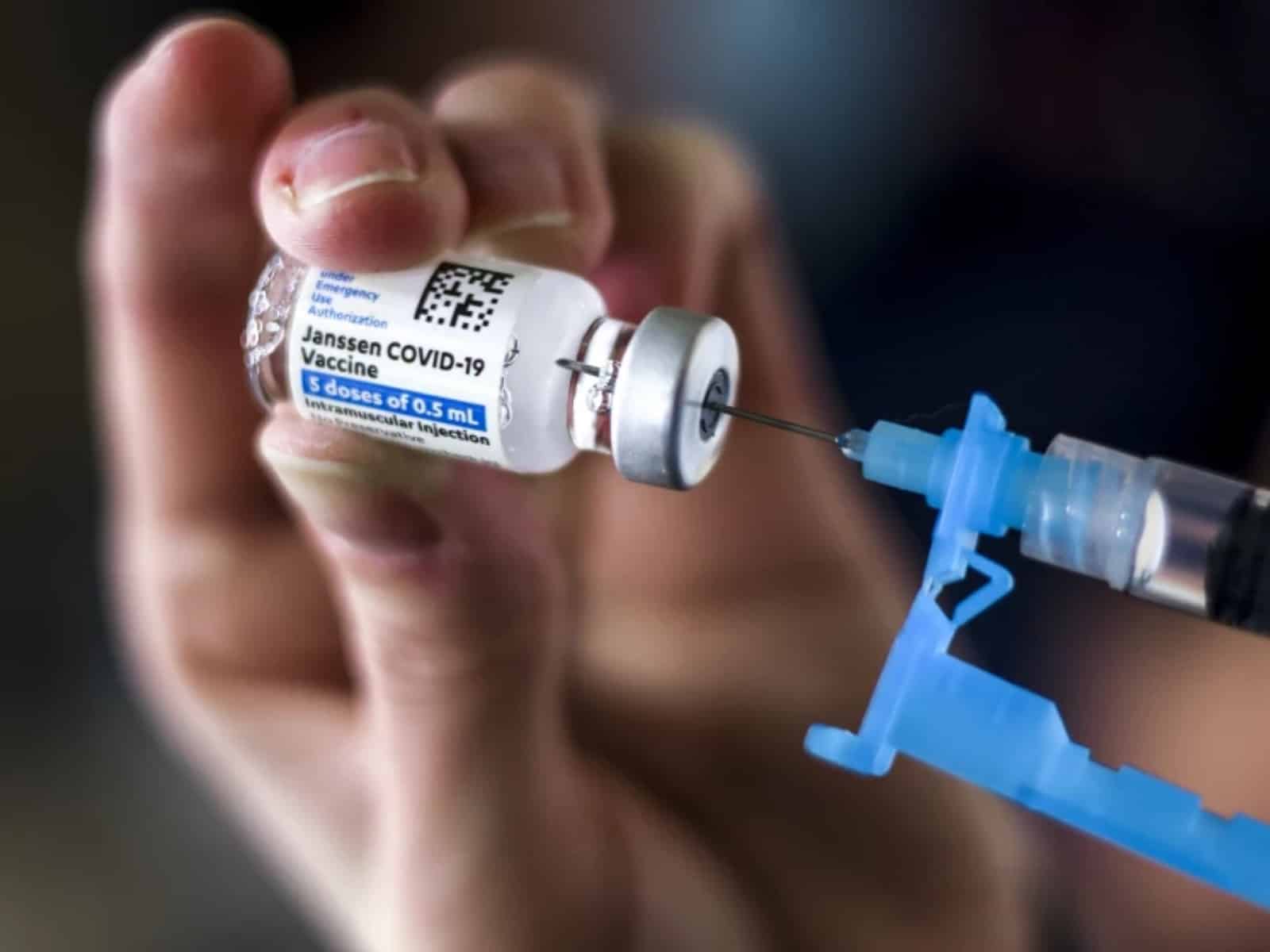
- El uso del fármaco se restringirá a personas mayores de 18 años de edad que, por razones de accesibilidad o clínicas, no pueden inmunizarse con otras dosis
La Administración de Alimentos y Fármacos (FDA, por sus siglas en inglés) informó que limitará el uso de la vacuna monodosis contra el covid-19 de Johnson & Johnson en Estados Unidos.
La decisión se tomó luego de revisar el riesgo de una condición de coagulación denominada síndrome de trombosis con trombocitopenia (TTS, por sus siglas en inglés), la cual se puede producir después de recibir la vacuna Janssen.
En este sentido, la agencia detalló en un comunicado que la autorización de emergencia del suero de Johnson & Johnson se restringirá a personas mayores de 18 años de edad para quienes otras vacunas contra el covid-19 autorizadas o aprobadas no son accesibles o clínicamente apropiadas.
Además, las personas mayores de 18 años que eligen la vacuna porque de otro modo no recibirán la inmunización contra el covid-19, también podrán recibir la de Johnson & Johnson.
Riesgos de coágulos de sangre
El doctor Peter Marks, director del Centro Evaluación e Investigación Biológica de la FDA, explicó que han estado vigilando de cerca la vacuna contra el covid-19 de Johnson & Johnson y la aparición del TTS tras su administración.
“Hemos utilizado la información actualizada de nuestros sistemas de vigilancia de la seguridad para revisar la autorización de uso de emergencia”, precisó en el comunicado.
La FDA detalló que después de realizar un análisis, una evaluación y una investigación actualizada de los casos notificados, determinaron que el riesgo de TTS, “un síndrome de coágulos de sangre raros y potencialmente mortales” en combinación con niveles bajos de plaquetas en la sangre, justifica la limitación del uso autorizado de la vacuna.
Indicó que los síntomas de esa afección inician aproximadamente una o dos semanas después de la administración de la vacuna.
No obstante, la FDA resaltó la rareza de la condición con 3,23 casos por cada millón de dosis de la vacuna administradas y nueve fallecimientos confirmados.
Hasta la fecha, en Estados Unidos se han administrado más de 18,7 millones de dosis de la vacuna de Johnson u0026amp; Johnson, según los Centros para el Control y la Prevención de Enfermedades (CDC, por sus siglas en inglés).
Marks agregó que reconocen que la vacuna de Johnson & Johnson todavía tiene un papel en la respuesta pandémica actual en los Estados Unidos y en toda la comunidad mundial.
Suspensión y reanudación del uso de la vacuna
El 13 abril de 2021, Estados Unidos detuvo el uso de la inyección de dosis única de Johnson & Johnson debido a algunos reportes de coagulación de la sangre en el cerebro entre mujeres después de recibir la vacuna.
Desde que se aprobó la vacuna en febrero, al menos 15 receptoras de la dosis sufrieron peligrosos coágulos de sangre, todas eran mujeres, la mayoría menores de 50 años.
A pocos días de finalizar el mes, las autoridades de salud de EE UU dieron el visto bueno a reanudar el uso de la vacuna Johnson & Johnson pero pidieron que se informe a los receptores sobre la posibilidad de que se formen coágulos de sangre.
Los CDC dijeron previamente en un comunicado que “se debe reanudar el uso de la vacuna en Estados Unidos” y que confían en que la vacuna es segura y eficaz para prevenir el covid-19. Además, agregaron que los trombos o coágulos de sangre son muy raros.
Tras una reunión celebrada en diciembre, el comité asesor sobre vacunas de los CDC recomendó como preferente el uso de las vacunas contra el covid-19 de ARNm como las Pfizer/BioNRech y Moderna, sobre la de Johnson u0026amp; Johnson.
El 15 % de los casos del síndrome han sido mortales
En una hoja informativa actualizada el 5 de mayo sobre la vacuna de Johnson & Johnson, la FDA afirmó que el 15 % de los casos de TTS han sido mortales. La agencia indicó que han confirmado 60 casos del síndrome.
La nueva advertencia de la FDA asegura que “la vacuna contra el covid-19 Janssen puede causar síndrome de trombosis con trombocitopenia que puede poner en peligro la vida”.
Aunque en general el riesgo de TTS es extremadamente raro, la tasa más alta se ha dado en mujeres de 30 a 49 años de edad. Al menos ocho casos por cada millón de dosis de vacunas administradas se han dado en mujeres de este grupo de edad.
En este sentido, la FDA insta a instruir a los beneficiarios de la vacuna contra el covid-19 de Johnson & Johnson para que busquen atención médica inmediata si presentan dificultad para respirar, dolor torácico, hinchazón de las piernas, dolor abdominal persistente, síntomas neurológicos (incluidos dolores de cabeza intensos o persistentes o visión borrosa), o petequias en el sitio de vacunación.